Ang mga peptide usa ka klase sa mga compound nga naporma pinaagi sa koneksyon sa daghang mga amino acid pinaagi sa peptide bond.Sila anaa sa tanang dapit sa buhing mga organismo.Hangtod karon, napulo ka libo nga mga peptide ang nakit-an sa buhi nga mga organismo.Ang mga peptide adunay importante nga papel sa pag-regulate sa functional nga mga kalihokan sa nagkalain-laing mga sistema, organo, tisyu ug mga selula ug sa mga kalihokan sa kinabuhi, ug kasagaran gigamit sa functional analysis, antibody research, drug development ug uban pang field.Uban sa pagpalambo sa biotechnology ug peptide synthesis nga teknolohiya, nagkadaghang peptide nga mga tambal ang naugmad ug gipadapat sa klinika.
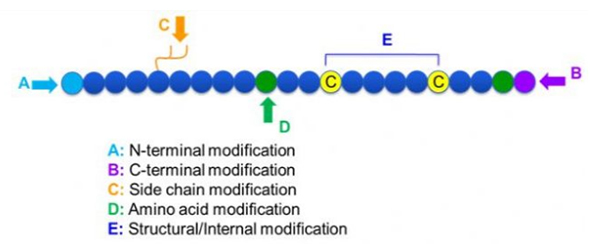
Adunay usa ka halapad nga lainlain nga mga pagbag-o sa peptide, nga mahimo ra bahinon sa pagbag-o sa post ug pagbag-o sa proseso (gamit ang gigikanan nga pagbag-o sa amino acid), ug pagbag-o sa N-terminal, pagbag-o sa C-terminal, pagbag-o sa side chain, pagbag-o sa amino acid, pagbag-o sa kalabera, ug uban pa, depende sa site sa pagbag-o (Figure 1).Ingon usa ka hinungdanon nga paagi aron mabag-o ang panguna nga istruktura sa kadena o mga grupo sa kilid nga kadena sa mga kadena sa peptide, ang pagbag-o sa peptide epektibo nga makabag-o sa pisikal ug kemikal nga mga kabtangan sa mga compound sa peptide, pagdugang sa pagkatunaw sa tubig, pagpalugway sa oras sa aksyon sa vivo, pagbag-o sa ilang biolohikal nga pag-apod-apod, pagwagtang sa immunogenicity. , pagpakunhod sa makahilo nga mga epekto, ug uban pa. Niini nga papel, daghang dagkong mga estratehiya sa pagbag-o sa peptide ug ang ilang mga kinaiya gipaila.
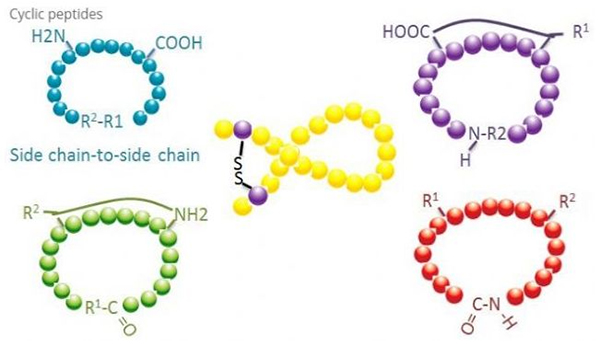
1. Cyclization
Ang mga cyclic peptides adunay daghang mga aplikasyon sa biomedicine, ug daghang mga natural nga peptide nga adunay biological nga kalihokan ang mga cyclic peptides.Tungod kay ang mga cyclic peptides lagmit nga mas estrikto kay sa linear peptides, sila hilabihan nga makasugakod sa digestive system, mabuhi sa digestive tract, ug magpakita sa mas lig-on nga kalambigitan alang sa target receptors.Ang cyclization mao ang labing direkta nga paagi sa pag-synthesize sa mga cyclic peptides, labi na sa mga peptide nga adunay dako nga structural skeleton.Sumala sa cyclization mode, kini mahimong bahinon ngadto sa side chain-side chain type, terminal - side chain type, terminal - terminal type (end to end type).
(1) sidechain-to-sidechain
Ang labing komon nga matang sa side-chain ngadto sa side-chain cyclization mao ang disulfide bridging tali sa cysteine residues.Kini nga cyclization gipaila pinaagi sa usa ka parisan sa mga residu sa cysteine nga gi-deprotect ug dayon gi-oxidize aron maporma ang disulfide bond.Ang polycyclic synthesis mahimong makab-ot pinaagi sa pinili nga pagtangtang sa mga grupo sa pagpanalipod sa sulfhydryl.Ang cyclization mahimo sa usa ka post-dissociation solvent o sa usa ka pre-dissociation resin.Ang cyclization sa mga resin mahimong dili kaayo epektibo kaysa solvent cyclization tungod kay ang mga peptide sa mga resin dili dali nga maporma ang cyclified conformation.Ang laing matang sa side-chain - side chain cyclization mao ang pagporma sa usa ka amide structure tali sa usa ka aspartic acid o glutamic acid residue ug base amino acid, nga nagkinahanglan nga ang side chain protection group kinahanglan nga mapili nga makuha gikan sa polypeptide. sa resin o pagkahuman sa dissociation.Ang ikatulo nga matang sa side-chain - side chain cyclization mao ang pagporma sa diphenyl ethers pinaagi sa tyrosine o p-hydroxyphenylglycine.Kini nga matang sa cyclization sa natural nga mga produkto makita lamang sa microbial nga mga produkto, ug ang mga produkto sa cyclization kasagaran adunay potensyal nga tambal nga bili.Ang pag-andam niini nga mga compound nanginahanglan talagsaon nga mga kondisyon sa reaksyon, mao nga dili kini kanunay nga gigamit sa synthesis sa naandan nga mga peptide.
(2) terminal-to-sidechain
Ang cyclization sa kadena sa kilid sa terminal kasagarang naglakip sa C-terminal nga adunay amino group sa lysine o ornithine nga side chain, o ang N-terminal nga adunay aspartic acid o glutamic acid side chain.Ang ubang polypeptide cyclization gihimo pinaagi sa pagporma sa ether bonds tali sa terminal C ug serine o threonine side chains.
(3) Terminal o head-to-tail type
Ang mga polypeptides sa kadena mahimo’g ma-cycle sa usa ka solvent o ma-fix sa usa ka resin pinaagi sa side chain cyclation.Ubos nga konsentrasyon sa peptides kinahanglan nga gamiton sa solvent sentralisasyon aron malikayan ang oligomerization sa peptides.Ang abot sa usa ka head-to-tail synthetic ring polypeptide nagdepende sa pagkasunod-sunod sa chain polypeptide.Busa, sa dili pa mag-andam sa mga cyclic peptides sa usa ka dako nga sukdanan, usa ka librarya sa posible nga kadena nga lead peptides kinahanglan una nga buhaton, gisundan sa cyclization aron makit-an ang pagkasunod-sunod nga adunay labing kaayo nga mga sangputanan.
2. N-methylation
Ang N-methylation orihinal nga mahitabo sa natural nga mga peptide ug gipaila sa peptide synthesis aron mapugngan ang pagporma sa hydrogen bonds, sa ingon naghimo sa mga peptide nga mas makasugakod sa biodegradation ug clearance.Ang synthesis sa mga peptide gamit ang N-methylated amino acid derivatives mao ang labing hinungdanon nga pamaagi.Dugang pa, ang reaksyon sa Mitsunobu sa N-(2-nitrobenzene sulfonyl chloride) polypeptide-resin intermediates nga adunay methanol mahimo usab nga gamiton.Kini nga pamaagi gigamit sa pag-andam sa cyclic peptide library nga adunay N-methylated amino acids.
3. Phosphorylation
Ang Phosphorylation usa sa labing kasagaran nga post-translational nga mga pagbag-o sa kinaiyahan.Sa mga selula sa tawo, labaw pa sa 30% sa mga protina ang phosphorylated.Ang phosphorylation, ilabi na ang mabalik nga phosphorylation, adunay importante nga papel sa pagkontrolar sa daghang mga proseso sa selula, sama sa signal transduction, gene expression, cell cycle ug cytoskeleton regulation, ug apoptosis.
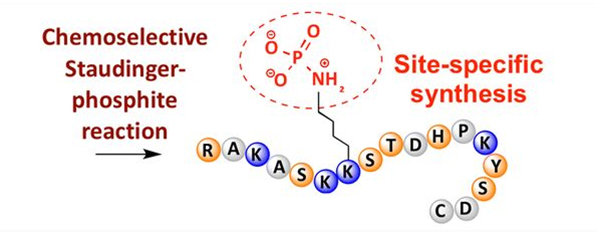
Ang phosphorylation mahimong maobserbahan sa lain-laing amino acid residues, apan ang labing komon nga phosphorylation target mao ang serine, threonine, ug tyrosine residues.Ang phosphotyrosine, phosphothreonine, ug phosphoserine derivatives mahimong ipasulod sa peptides atol sa synthesis o maporma human sa peptide synthesis.Ang pinili nga phosphorylation mahimong makab-ot gamit ang mga residue sa serine, threonine, ug tyrosine nga pilion nga nagtangtang sa mga grupo sa pagpanalipod.Ang ubang mga phosphorylation reagents mahimo usab nga ipaila ang phosphoric acid nga mga grupo ngadto sa polypeptide pinaagi sa post modification.Sa bag-ohay nga mga tuig, ang site-specific phosphorylation sa lysine nakab-ot gamit ang usa ka chemically selective Staudinger-phosphite reaction (Figure 3).
4. Myristoylation ug palmitoylation
Ang acylation sa N-terminal nga adunay mga fatty acid nagtugot sa mga peptide o mga protina sa pagbugkos sa mga lamad sa selula.Ang myridamoylated sequence sa N-terminal makapahimo sa Src family protein kinases ug reverse transcriptase Gaq proteins nga mapuntirya sa paggapos sa cell membranes.Ang myristic acid nalambigit sa N-terminal sa resin-polypeptide gamit ang standard coupling reactions, ug ang resulta nga lipopeptide mahimong ma-dissociated ubos sa standard nga kondisyon ug maputli sa RP-HPLC.
5. Glycosylation
Glycopeptides sama sa vancomycin ug teicolanin importante nga mga antibiotics alang sa pagtambal sa mga drug-resistant bacterial infections, ug uban pang mga glycopeptides sagad gigamit sa pagdasig sa immune system.Dugang pa, tungod kay daghang mga microbial antigens ang glycosylated, kini adunay dakong importansya sa pagtuon sa glycopeptides alang sa pagpalambo sa terapyutik nga epekto sa impeksyon.Sa laing bahin, nakit-an nga ang mga protina sa cell lamad sa mga selula sa tumor nagpakita sa abnormal nga glycosylation, nga naghimo sa glycopeptides nga adunay hinungdanon nga papel sa panukiduki sa pagdepensa sa resistensya sa kanser ug tumor.Ang mga glycopeptide giandam pinaagi sa Fmoc/t-Bu nga pamaagi.Glycosylated residues, sama sa threonine ug serine, sagad gipaila ngadto sa polypeptides pinaagi sa pentafluorophenol ester activated fMOCs sa pagpanalipod sa glycosylated amino acids.
6. Isoprene
Ang isopentadienylation mahitabo sa mga residu sa cysteine sa kilid nga kadena duol sa C-terminal.Ang isoprene sa protina makapauswag sa pagkadugtong sa cell lamad ug makaporma sa interaksyon sa protina-protina.Ang mga isopentadienated nga protina naglakip sa tyrosine phosphatase, gamay nga GTase, mga molekula sa cochaperone, nukleyar nga lamina, ug mga protina nga nagbugkos sa centromeric.Ang isoprene polypeptides mahimong maandam gamit ang isoprene sa mga resin o pinaagi sa pagpaila sa mga derivatives sa cysteine.
7. Pagbag-o sa polyethylene glycol (PEG).
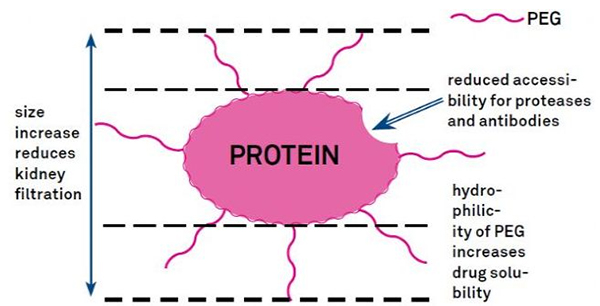
Ang pagbag-o sa PEG mahimong magamit aron mapauswag ang kalig-on sa hydrolytic sa protina, biodistribution ug pagkatunaw sa peptide.Ang pagpaila sa mga kadena sa PEG ngadto sa mga peptide makapauswag sa ilang mga kabtangan sa pharmacological ug makapugong usab sa hydrolysis sa mga peptide pinaagi sa mga proteolytic enzymes.Ang PEG peptides moagi sa glomerular capillary cross section nga mas dali kay sa ordinaryo nga mga peptide, nga makapakunhod pag-ayo sa renal clearance.Tungod sa taas nga aktibo nga katunga sa kinabuhi sa mga peptide sa PEG sa vivo, ang normal nga lebel sa pagtambal mahimong mapadayon sa mas mubu nga mga dosis ug dili kaayo kanunay nga mga tambal nga peptide.Bisan pa, ang pagbag-o sa PEG adunay negatibo nga epekto.Ang daghang kantidad sa PEG makapugong sa enzyme sa pagdaot sa peptide ug makapakunhod usab sa pagbugkos sa peptide sa target nga receptor.Apan ang ubos nga affinity sa PEG peptides kasagarang gibawi sa ilang mas taas nga pharmacokinetic half-life, ug pinaagi sa pagkaanaa sa lawas nga mas dugay, ang PEG peptides adunay mas dako nga posibilidad nga masuhop sa target nga mga tisyu.Busa, ang PEG polymer specifications kinahanglan nga ma-optimize alang sa kamalaumon nga mga resulta.Sa laing bahin, ang PEG peptides natipon sa atay tungod sa pagkunhod sa renal clearance, nga miresulta sa macromolecular syndrome.Busa, ang mga pagbag-o sa PEG kinahanglan nga gidisenyo nga labi ka mabinantayon kung ang mga peptide gigamit alang sa pagsulay sa droga.
Ang kasagarang mga grupo sa pagbag-o sa PEG modifiers mahimong halos i-summarize sama sa mosunod: Amino (-amine) -NH2, aminomethyl-Ch2-NH2, hydroxy-OH, carboxy-Cooh, sulfhydryl (-Thiol) -SH, Maleimide -MAL, succinimide carbonate - SC, succinimide acetate -SCM, succinimide propionate -SPA, n-hydroxysuccinimide -NHS, Acrylate-ch2ch2cooh, aldehyde -CHO (sama sa propional-ald, butyrALD), acrylic base (-acrylate-acrl), azido-azide, biotinyl - Biotin, Fluorescein, glutaryl -GA, Acrylate Hydrazide, alkyne-alkyne, p-toluenesulfonate -OTs, succinimide succinate -SS, ug uban pa. Ang PEG derivatives nga adunay carboxylic acid mahimong iupod sa n-terminal amines o lysine side chains.Amino-activate PEG mahimong inubanan sa aspartic acid o glutamic acid kilid kadena.Ang mal-activate nga PEG mahimong i-conjugated sa mercaptan sa hingpit nga deprotected cysteine side chains [11].Ang mga modifier sa PEG kasagarang giklasipikar ingon sa mosunod (nota: ang mPEG mao ang methoxy-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) tul-id nga kadena nga PEG modifier
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OTs, mPEG-SH, mPEG-ALD, mPEG-butyrALD, mPEG-SS
(2) bifunctional nga PEG modifier
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) branching PEG modifier
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinization
Ang biotin mahimong lig-on nga gigapos sa avidin o streptavidin, ug ang kusog sa pagbugkos hapit sa covalent bond.Ang mga peptide nga adunay label sa biotin kasagarang gigamit sa immunoassay, histocytochemistry, ug fluorescence-based flow cytometry.Ang gimarkahan nga antibiotin antibodies mahimo usab nga gamiton sa pagbugkos sa biotinylated peptides.Ang mga label sa biotin sagad nga gilakip sa lysine side chain o sa N terminal.Ang 6-aminocaproic acid sagad gigamit isip usa ka bugkos tali sa peptides ug biotin.Ang bugkos flexible sa pagbugkos sa substrate ug mas maayo nga nagbugkos sa presensya sa steric hindrance.
9. Pag-label sa fluorescent
Ang pag-label sa fluorescent mahimong magamit sa pagsubay sa mga polypeptide sa buhi nga mga selula ug sa pagtuon sa mga enzyme ug mga mekanismo sa paglihok.Ang Tryptophan (Trp) kay fluorescent, mao nga magamit kini alang sa intrinsic nga pag-label.Ang emission spectrum sa tryptophan nagdepende sa peripheral nga palibot ug mikunhod uban ang pagkunhod sa polarity sa solvent, usa ka kabtangan nga mapuslanon sa pag-ila sa istruktura sa peptide ug paggapos sa receptor.Ang tryptophan fluorescence mahimong mapalong pinaagi sa protonated aspartic acid ug glutamic acid, nga mahimong limitahan ang paggamit niini.Ang grupo sa Dansyl chloride (Dansyl) kay fluorescent kaayo kung gigapos sa usa ka amino group ug sagad gigamit isip usa ka fluorescent nga label sa mga amino acid o protina.
Ang fluorescence resonance Energy conversion (FRET) mapuslanon alang sa mga pagtuon sa enzyme.Kung gigamit ang FRET, ang substrate nga polypeptide kasagaran adunay usa ka grupo sa pag-label sa fluorescence ug usa ka grupo sa pagpalong sa fluorescence.Ang gimarkahan nga fluorescent nga mga grupo gipalong sa quencher pinaagi sa non-photon energy transfer.Kung ang peptide mabulag gikan sa enzyme nga gikuwestiyon, ang grupo sa pag-label nagpagawas sa fluorescence.
10. Cage polypeptides
Ang mga peptide sa hawla adunay optically removable protective nga mga grupo nga nanalipod sa peptide gikan sa pagbugkos sa receptor.Kung naladlad sa radiation sa UV, ang peptide gi-aktibo, gipahiuli ang pagkadugtong niini sa receptor.Tungod kay kini nga optical nga pagpaaktibo mahimong kontrolado sumala sa oras, amplitude, o lokasyon, ang mga peptide sa hawla mahimong magamit sa pagtuon sa mga reaksyon nga nahitabo sa mga selyula.Ang labing sagad nga gigamit nga mga grupo sa pagpanalipod alang sa mga polypeptide sa hawla mao ang 2-nitrobenzyl nga mga grupo ug ang ilang mga gigikanan, nga mahimo’g ipaila sa synthesis sa peptide pinaagi sa pagpanalipod sa mga gigikanan sa amino acid.Ang mga derivatives sa amino acid nga naugmad mao ang lysine, cysteine, serine, ug tyrosine.Ang aspartate ug glutamate derivatives, bisan pa, dili kasagarang gigamit tungod sa ilang pagkadaling madala sa cyclization sa panahon sa peptide synthesis ug dissociation.
11. Polyantigenic peptide (MAP)
Ang mugbo nga mga peptide kasagaran dili immune ug kinahanglan nga iupod sa mga protina sa carrier aron makahimo og mga antibodies.Ang polyantigenic peptide (MAP) gilangkuban sa daghang managsama nga mga peptide nga konektado sa lysine nuclei, nga espesipikong makapahayag sa taas nga potency immunogens ug magamit sa pag-andam sa peptide-carrier protein couplets.Ang MAP polypeptides mahimong ma-synthesize pinaagi sa solid phase synthesis sa MAP resin.Bisan pa, ang dili kompleto nga pagdugtong nagresulta sa nawala o naputol nga mga kadena sa peptide sa pipila nga mga sanga ug sa ingon wala magpakita sa mga kabtangan sa orihinal nga polypeptide sa MAP.Isip usa ka alternatibo, ang mga peptide mahimong andamon ug putli nga gilain ug dayon iupod sa MAP.Ang han-ay sa peptide nga gilakip sa peptide core maayo nga gipasabut ug dali nga gihulagway pinaagi sa mass spectrometry.
Konklusyon
Ang pagbag-o sa peptide usa ka hinungdanon nga paagi sa pagdesinyo sa mga peptide.Ang mga peptide nga giusab sa kemikal dili lamang makapadayon sa taas nga biolohikal nga kalihokan, apan epektibo usab nga malikayan ang mga kakulangan sa immunogenicity ug toxicity.Sa parehas nga oras, ang pagbag-o sa kemikal mahimo’g maghatag mga peptide sa pipila ka bag-ong maayo kaayo nga mga kabtangan.Sa bag-ohay nga mga tuig, ang pamaagi sa CH activation alang sa post-modification sa polypeptides paspas nga naugmad, ug daghang importante nga mga resulta ang nakab-ot.
Oras sa pag-post: Mar-20-2023
